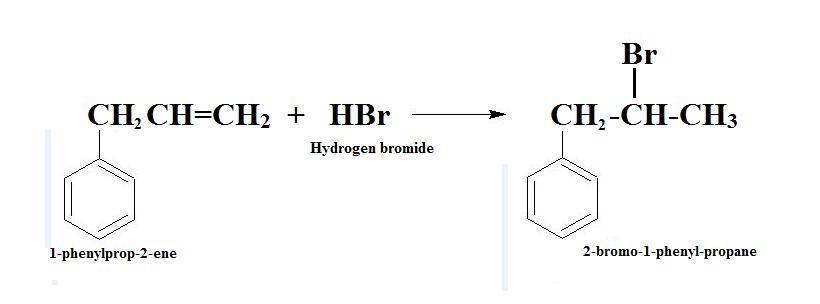
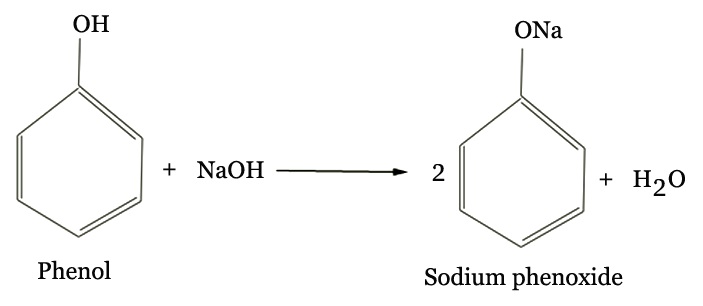
Phản ứng trên là phản ứng brom hóa của toluen. Trong phản ứng, brom được thêm vào toluen để thay thế nhóm mety bằng nhóm brom. Kết quả của phản ứng là sản phẩm là bromua metyl benzene (C6H5CH2Br) và axit hydrobromic (HBr). Phản ứng này là một phản ứng hữu cơ quan trọng để tạo ra các hợp chất hữu cơ chứa halogen.
Mục lục bài viết
- 1 1. Phản ứng khi cho Toluen tác dụng với Br2 (ánh sáng) theo tỉ lệ mol 1:1
- 2 2. Toluen tác dụng với Br2 điều kiện có bột sắt:
- 3 3. Tính chất hóa học của Toluen:
- 3.1 3.1. Một trong những phản ứng quan trọng của toluen là phản ứng với chất brom khan:
- 3.2 3.2. Toluen cũng có thể phản ứng với khí clo trong điều kiện có sự xúc tác của ánh sáng, để tạo ra diclometan và axit HCl theo phương trình:
- 3.3 3.3. Toluen cũng có khả năng tham gia phản ứng nitro hóa để tạo ra nitrotoluen và nước:
- 3.4 3.4. Toluen còn có thể phản ứng cộng với H2 để tạo ra metylxiclohexan:
- 4 4. Câu hỏi bài tập liên quan:
1. Phản ứng khi cho Toluen tác dụng với Br2 (ánh sáng) theo tỉ lệ mol 1:1
C6H5CH3 + Br2 C6H5CH2Br + HBr
Khi toluen phản ứng với Br2 trong điều kiện ánh sáng, có thể xảy ra nhiều phản ứng khác nhau. Chẳng hạn, phản ứng thế trên nhánh tạo ra bezyl bromua như đã được đề cập trong bài viết. Tuy nhiên, cũng có thể xảy ra phản ứng thế trên vòng tạo ra sản phẩm khác. Ngoài ra, phản ứng xảy ra có thể phụ thuộc vào nhiều yếu tố khác như nhiệt độ, áp suất, độ tinh khiết của các chất tham gia.
Sau khi phản ứng xảy ra, sản phẩm thu được có thể được tách ra và tinh chế bằng nhiều phương pháp khác nhau. Ví dụ, sản phẩm có thể được chiết ra bằng dung môi, hoặc được tách riêng từ các chất còn lại bằng phương pháp sử dụng tính khác nhau của các chất trong hỗn hợp.
Vì vậy, phản ứng giữa toluen và Br2 là một phản ứng có nhiều yếu tố phức tạp và có thể dẫn đến nhiều sản phẩm khác nhau
2. Toluen tác dụng với Br2 điều kiện có bột sắt:
Nếu cho toluen phản ứng với brom trong điều kiện có bột sắt, quá trình sẽ tạo ra một hỗn hợp sản phẩm chứa các hợp chất thế brom, với các chất này tập trung chủ yếu vào vị trí para và ortho. Điều này có nghĩa là trong hỗn hợp sản phẩm, các phân tử sẽ có các nhóm brom liên kết với các nguyên tử cacbon tại vị trí para hoặc ortho. Việc tách hỗn hợp này và phân tích các sản phẩm có thể được thực hiện bằng các phương pháp hóa học khác nhau, chẳng hạn như sắc ký hoặc phổ hấp thụ. Vì vậy, quá trình này có thể được sử dụng để sản xuất các hợp chất hữu cơ phức tạp hơn, cho phép các nhà khoa học nghiên cứu các tính chất và ứng dụng của chúng.
3. Tính chất hóa học của Toluen:
Toluen là một hợp chất hữu cơ quan trọng trong ngành công nghiệp hóa chất và được sử dụng rộng rãi trong sản xuất các sản phẩm như thuốc nhuộm, nhựa, thuốc trừ sâu và nhiên liệu động cơ. Điều đó đặt ra một yêu cầu lớn đối với việc hiểu rõ về tính chất và các phản ứng của toluen.
3.1. Một trong những phản ứng quan trọng của toluen là phản ứng với chất brom khan:
Khi phản ứng này xảy ra, brom toluen và axit HBr được tạo ra theo phương trình hóa học sau:
Br2 + C6H5CH3 → C6H5CH2Br + HBr
3.2. Toluen cũng có thể phản ứng với khí clo trong điều kiện có sự xúc tác của ánh sáng, để tạo ra diclometan và axit HCl theo phương trình:
Cl2 + C6H5CH3 → HCl + C6H5CH2Cl
3.3. Toluen cũng có khả năng tham gia phản ứng nitro hóa để tạo ra nitrotoluen và nước:
C6H5CH3 + HNO3 → C6H4NO2CH3 + H2O
3.4. Toluen còn có thể phản ứng cộng với H2 để tạo ra metylxiclohexan:
2C6H5CH3 + 7H2 → 2C6H12CH3
Tuy nhiên, phản ứng oxy hóa với nhóm metyl là một trong những phản ứng quan trọng nhất của toluen. Khi toluen phản ứng oxy hóa với nhóm metyl, sẽ tạo ra nhiều sản phẩm khác nhau với tính chất khác nhau. Điều này có thể gây ra tác động đáng kể đến chất lượng sản phẩm cuối cùng.
Tóm lại, toluen là một hợp chất quan trọng trong ngành công nghiệp hóa chất và có thể tham gia vào nhiều phản ứng khác nhau để tạo ra các sản phẩm mới. Việc hiểu rõ về các tính chất và phản ứng của toluen là rất quan trọng để đảm bảo chất lượng sản phẩm cuối cùng.
4. Câu hỏi bài tập liên quan:
Câu 1. Đốt cháy hòa toàn 7,8 gam benzen rồi hấp thụ sản phẩm cháy vào bình đựng dung dịch nước vôi trong dư. Khối lượng dung dịch tăng hay giảm bao nhiêu gam?
A. tăng 56,4 gam.
B. giảm 28,2 gam.
C. giảm 56,4 gam.
D. tăng 28,2 gam.
Đáp án B
Trong phản ứng hóa học, nC6H6 tương đương với 0,1 mol.
Phương trình hóa học của phản ứng:
C6H6+ 15/2O2 6CO2 + 3H2O
Sau phản ứng, số mol C6H6 đã giảm xuống còn 0,3 mol.
0,6 mol CO2 được sinh ra trong quá trình phản ứng, và kết hợp với Ca(OH)2 để tạo thành CaCO3 và H2O:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Sau phản ứng, ta thu được 0,6 mol CaCO3 tương đương với khối lượng 60g.
Trong quá trình phản ứng, cũng tạo ra 0,6 mol CO2 và 0,3 mol H2O. Khối lượng của chúng là:
mCO2 = 0,6.44 = 26,4 (g)
mH2O = 0,3.18 = 5,4 (g)
Vậy khối lượng của CO2 và H2O kết hợp là 31,8g.
Do đó, khối lượng dung dịch giảm là 60g – 31,8g = 28,2g.
Câu 2. Dãy đồng đẳng benzen có công thức chung là
A.CnH2n+2
B. CnH2n-2
C. CnH2n-4
D. CnH2n-6
Đáp án D
Câu 3. Công thức phân tử của Strien là
A.C6H6
B. C7H8
C. C8H8
D. C8H10
Đáp án C
Câu 4. Công thức phân tử của toluen là
A.C6H6
B. C7H8
C. C8H8
D. C8H10
Đáp án B
Câu 5. Nhận xét nào sau đây đúng?
A. Benzen và đồng đẳng của benzen chỉ có khả năng tham gia phản ứng cộng.
B. Benzen và đồng đẳng của benzen chỉ có khả năng tham gia phản ứng thế.
C. Benzen và đồng đẳng của benzen vừa có khả năng tham gia phản ứng cộng, vừa có khả năng tham gia phản ứng thế.
D. Benzen và đồng đẳng của benzen không có khả năng tham gia phản ứng cộng và phản ứng thế.
Đáp án B
Câu 6. Benzen tác dụng với Br2 theo tỷ lệ mol 1 : 1 (có mặt bột Fe), thu được sẩn phẩm hữu cơ là
A.C6H6Br2
B. C6H6Br6
C. C6H5Br
D. C6H6Br44
Đáp án C
Câu 7. Toluen tác dụng với Br2 chiếu sáng (tỷ lệ mol 1 : 1), thu được sẩn phẩm hữu cơ là
A. o-bromtoluen
B. m-bromtoluen.
C. phenylbromua
D. benzylbromua
Đáp án D
Khi sử dụng xúc tác bột sắt Fe, brom (Br) sẽ thay thế hydro (H) ở vòng phản ứng. Điều này có thể được giải thích bằng cách cho rằng sự hấp thụ ánh sáng có thể làm tăng năng lượng của các phân tử Br2, dẫn đến sự phân hủy và giải phóng các radicô gốc Br. Những radicô gốc này sẽ gia nhập vào phản ứng vòng và tham gia phản ứng thế vào H, tạo ra sản phẩm phản ứng. Trong khi đó, khi chiếu sáng, Br cũng có thể thay thế H ở nhánh phản ứng, tuy nhiên, cơ chế chính xác của quá trình này vẫn chưa được hiểu rõ. Tuy nhiên, điều này lại là một trong những điểm hấp dẫn của nghiên cứu hóa học, vì vẫn còn nhiều câu hỏi chưa được giải đáp trong lĩnh vực này.
Câu 8. Cho toluen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế 2,4,6-trinitrotoluen (TNT). KHối lượng điều chế được từ 23 kg toluen (hiệu suất 80%)là
A. 45,40 kg
B. 70,94 kg
C. 18,40 kg
D. 56,75 kg
Đáp án A
C6H5CH3 + 3HONO2 → C6H5(NO2)3CH3 + 3H2O
92 gam 227 gam (H= 100%)
23 kg m kg (H = 80%)
m = 23.227/92 .80% = 45,4 kg
Câu 9. Khi cho một ít benzen vào ống nghiệm đựng nước brom, lắc nhẹ. Hiện tượng quan sát được là:
A. nước brom mất màu, thu được chất lỏng đồng nhất
B. chất lỏng trong ống nghiệm chia thành 2 lớp: lớp có màu đỏ và lớp không màu
C. chất lỏng trong ống nghiệm không thay đổi
D. nước brom mất màu, có chất lỏng không tan chìm xuống đáy ống nghiệm
Đáp án B
Benzen là một hợp chất hữu cơ không màu, có mùi đặc trưng, được sử dụng trong sản xuất các hợp chất hữu cơ, như dầu mỡ, dược phẩm, thuốc nhuộm và chất tẩy rửa. Khi cho benzen vào ống nghiệm chứa nước brom, chúng ta sẽ quan sát được hiện tượng tách lớp của hai chất. Điều này do benzen không tác dụng với nước brom, do đó chất lỏng trong ống nghiệm sẽ tách thành hai lớp khác nhau: Lớp chất lỏng trên là dung dịch brom trong benzen có màu vàng, do benzen tan trong brom tạo nên. Lớp dưới là nước trong suốt, có thể quan sát được dễ dàng.
Điều này giúp chúng ta hiểu được tính chất vật lý và hóa học của benzen. Benzen là một hợp chất không phân cực, do đó có thể tan trong các dung môi hữu cơ và không tan trong nước. Trong khi đó, nước brom là một chất phân cực, tức là có khả năng tương tác với nước. Do đó, khi cho benzen vào nước brom, hai chất sẽ không tương tác với nhau và tách lớp như mô tả ở trên.
Phương pháp này đã được sử dụng để phân biệt benzen với các hợp chất hữu cơ khác, đồng thời cũng được sử dụng trong các thí nghiệm hóa học để xác định tính chất vật lý và hóa học của các hợp chất khác nhau. Ngoài ra, việc hiểu thêm về tính chất và phản ứng của benzen cũng giúp chúng ta áp dụng nó trong các ứng dụng khác nhau trong lĩnh vực công nghiệp và y học.
Câu 10. Cho benzen tác dụng với hidro dư, có xúc tác thu được xiclohexan (C6H12). Điều đó chứng tỏ:
A. phân tử benzen có mạch vòng, có 3 liên kết đôi C=C
B. Benzen là hidrocacbon mạch hở có 3 liên kết đôi C=C
C. Phân tử benzen có cấu tạo vòng phẳng
D. phân tử benzen có cấu tạo mạch hở, không phân nhánh.
Đáp án A
Cho benzen tác dụng với hidro dư, có xúc tác thu được xiclohexan (C6H12). Điều đó chứng tỏ: phân tử benzen có mạch vòng, có 3 liên kết đôi C=C
Câu 11. Hiện tượng gì xảy ra khi đun nóng toluen với dung dịch thuốc tím?
A. Dung dịch KMnO4 bị mất màu.
B. Có kết tủa trắng.
C. Có sủi bọt khí.
D. Không có hiện tượng gì.
Đáp án A
Hiện tượng xảy ra khi đun nóng toluen với dung dịch thuốc tím là dung dịch KMnO4 bị mất màu.
C6H5CH3 + 2KMnO4 → H2O + KOH + 2MnO2+ C6H5COOK
Câu 12. Dãy các chất đều làm mất màu dung dịch nước brom là
A. C2H2, C6H6, CH4.
B. C2H2, CH4, C2H4.
C. C2H2, C2H4.
D. C2H2, H2, CH4.
Đáp án C
Dựa vào tính chất hóa học của các hợp chất đã học.
Dãy các chất đều làm mất màu dung dịch nước brom là C2H2, C2H4.
Hương trình hóa học
C2H2 + 2Br2 → C2H2Br4
C2H4 + Br2→ C2H4Br2
Câu 13. Dãy chất nào sau đây gồm các chất làm mất màu dung dịch nước brom?
A. Axeton, axit fomic, fomanđehit.
B. Propanal, axit fomic, etyl axetat
C. Etanal, propanon, etyl fomat.
D. Etanal, axit fomic, etyl fomat.
Đáp án D
Etanol (CH3CHO); axit fomic (HCOOH); etylfomat (HCOOC2H5) đều có tính khử (của -CHO) nên đều có phản ứng với Br2