Phản ứng giữa etilen (C2H4) và nước (H2O) tạo ra etylic (C2H5OH) theo phương trình hóa học sau: C2H4 + H2O → C2H5OH.
Mục lục bài viết
1. Tính chất của phản ứng C2H4 + H2O → C2H5OH:
Phản ứng giữa etilen (C2H4) và nước (H2O) tạo ra etylic (C2H5OH) theo phương trình hóa học sau: C2H4 + H2O → C2H5OH
Đây là một phản ứng trùng hợp giữa hai chất không có liên kết hóa học trước đó, trong đó hai chất tạo thành một chất duy nhất. Phản ứng này xảy ra trong điều kiện nhiệt độ và áp suất cao, thông qua quá trình thủy phân.
Etylen (C2H4) là một hợp chất hữu cơ không màu, không mùi và không tan trong nước. Nó có cấu trúc phân tử là một liên kết ba, với hai nguyên tử cacbon liên kết với nhau và mỗi nguyên tử cacbon liên kết với hai nguyên tử hydro (H).
Khi etilen (C2H4) phản ứng với nước (H2O), các phân tử etilen và nước cùng tham gia vào quá trình, trong đó etylen bị thủy phân để tạo thành etylic (C2H5OH) và nước bị oxi hóa thành khí oxi) và khí hydro (H2).
Công thức hóa học của phản ứng thủy phân etylen và nước là: C2H4 + H2O → C2H5OH + O + H2
Tuy nhiên, trong điều kiện thực tế, phản ứng này chỉ tạo ra etylic và một sản phẩm phụ là oxit của cacbon (CO).
Quá trình thực hiện phản ứng trên được thực hiện trong một bình kín, trong đó etylen và nước được đưa vào bình và đun nóng ở nhiệt độ khoảng 300 độ C và áp suất khoảng 60-70 atm. Quá trình này tạo ra etylic và sản phẩm phụ CO.
Phản ứng thủy phân etylen và nước được sử dụng để sản xuất rượu etylic, một hợp chất hữu cơ quan trọng được sử dụng trong ngành công nghiệp hóa chất, sản xuất xăng, thuốc lá và các sản phẩm dược phẩm khác.
Trong công nghiệp, phương pháp sản xuất rượu etylic từ etilen và nước được sử dụng rộng rãi, vì nó cho phép sản xuất rượu với số lượng lớn, đồng thời tiết kiệm chi phí và năng lượng sản xuất. Tuy nhiên, quá trình sản xuất rượu etylic từ phản ứng thủy phân etylen và nước cần được thực hiện trong điều kiện nhiệt độ, áp suất và cân bằng hóa học phù hợp để đạt được hiệu quả sản xuất cao nhất.
2. Điều kiện xảy ra phản ứng C2H4 + H2O → C2H5OH:
Phản ứng C2H4 + H2O → C2H5OH là một phản ứng hóa học quan trọng trong ngành công nghiệp hóa chất. Phản ứng này được sử dụng để sản xuất rượu etylic (C2H5OH), một chất rất phổ biến và có nhiều ứng dụng trong cuộc sống.
Để xảy ra phản ứng C2H4 + H2O → C2H5OH, cần có một số điều kiện sau:
2.1. Điều kiện nhiệt độ:
Phản ứng xảy ra ở nhiệt độ cao, thường trong khoảng từ 150°C đến 300°C. Nhiệt độ cao giúp tăng tốc độ phản ứng và giảm thời gian cần thiết để sản xuất sản phẩm.
2.2. Điều kiện áp suất:
Áp suất ở mức trung bình, tùy thuộc vào điều kiện nhiệt độ và nguyên liệu sử dụng. Áp suất phù hợp sẽ tạo ra điều kiện lý tưởng để phản ứng xảy ra một cách hiệu quả.
2.3. Điều kiện chất xúc tác:
Phản ứng xảy ra nhanh hơn và đạt hiệu suất cao hơn khi có chất xúc tác. Các chất xúc tác thường được sử dụng là H3PO4, Al2O3, ZnO, Cr2O3, MgO, v.v. Chất xúc tác giúp tăng độ bền của sản phẩm và tăng khả năng tái sử dụng của chúng.
2.4. Điều kiện nguyên liệu:
Ngoài ra, phản ứng C2H4 + H2O → C2H5OH còn yêu cầu sự có mặt của nguyên liệu đầu vào là etylen (C2H4) và nước (H2O).
Điều kiện trên đây rất quan trọng để đảm bảo rằng phản ứng xảy ra đúng cách và thu được sản phẩm chất lượng cao. Sử dụng các điều kiện phù hợp cũng sẽ giúp tăng hiệu suất sản xuất và giảm chi phí đầu tư cho quá trình sản xuất.
3. Ứng dụng của phản ứng C2H4 + H2O → C2H5OH:
Phản ứng C2H4 + H2O → C2H5OH là phản ứng trùng hợp giữa etylen và nước để tạo ra ethanol. Đây là một phản ứng quan trọng trong ngành công nghiệp hóa chất và có nhiều ứng dụng khác nhau trong cuộc sống hàng ngày của chúng ta.
Một trong những ứng dụng quan trọng nhất của phản ứng này là trong sản xuất nhiên liệu sinh học. Ethanol là một loại nhiên liệu sinh học thay thế cho xăng và dầu diesel, được sản xuất từ nguồn nguyên liệu tái tạo như cây mía đường, bắp, lúa mạch và cỏ. Sử dụng ethanol như một nhiên liệu sinh học giúp giảm thiểu ô nhiễm môi trường đồng thời cung cấp một nguồn nhiên liệu tái tạo và giúp giảm sự phụ thuộc vào dầu mỏ.
Ngoài ra, ethanol cũng được sử dụng để sản xuất các hợp chất hóa học khác như axit axetic, acetaldehyd, ethyl acetate và ethylamine. Các hợp chất này được sử dụng trong nhiều ngành công nghiệp khác nhau, bao gồm sản xuất thuốc, dược phẩm, sơn và chất tẩy rửa.
Ethanol còn được sử dụng trong sản xuất nhiều sản phẩm chăm sóc cá nhân. Nó được sử dụng làm thành phần chính trong nước hoa, sữa tắm và kem đánh răng. Với tính chất kháng khuẩn, ethanol thường được sử dụng để tẩy rửa và khử trùng.
Cuối cùng, ethanol cũng được sử dụng để sản xuất một số loại thực phẩm như nước giải khát, bia và rượu. Với tính chất tạo nên hương vị đặc biệt, ethanol đóng vai trò quan trọng trong việc sản xuất các loại đồ uống này.
Tóm lại, phản ứng C2H4 + H2O → C2H5OH là một phản ứng quan trọng trong ngành công nghiệp hóa chất với nhiều ứng dụng khác nhau trong cuộc sống hàng ngày của chúng ta. Từ việc sản xuất nhiên liệu sinh học, hóa chất, sản phẩm chăm sóc cá nhân cho đến thực phẩm, ethanol đóng vai trò quan trọng và không thể thiếu trong nhiều lĩnh vực khác nhau của cuộc sống.
4. Bài tập trắc nhiệm liên quan:
Câu 1. Ancol etylic có thể phản ứng được với các chất trong dãy nào dưới đây:
A. K, HBr, Fe.
B. Na, CuO, NaOH.
C. Na, CuO, HCl.
D. Na, MgCO3, HCl.
Câu 2. Trong phân tử etilen giữa hai nguyên tử cacbon có
A. hai liên kết đôi.
B. một liên kết đôi.
C. một liên kết đơn.
D. một liên kết ba.
Câu 3. Etilen có tính chất vật lý nào sau đây?
A. là chất khí không màu, không mùi, tan nhiều trong nước, nhẹ hơn không khí.
B. là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. là chất khí màu vàng lục, mùi xốc, ít tan trong nước, nặng hơn không khí.
D. là chất khí không màu, mùi hắc, tan trong nước, nặng hơn không khí.
Câu 4. Khi đốt cháy khí etilen thì số mol CO2 và H2O được tạo thành theo tỉ lệ
A. 2 : 1.
B. 1 : 2.
C. 1 : 3.
D. 1 : 1.
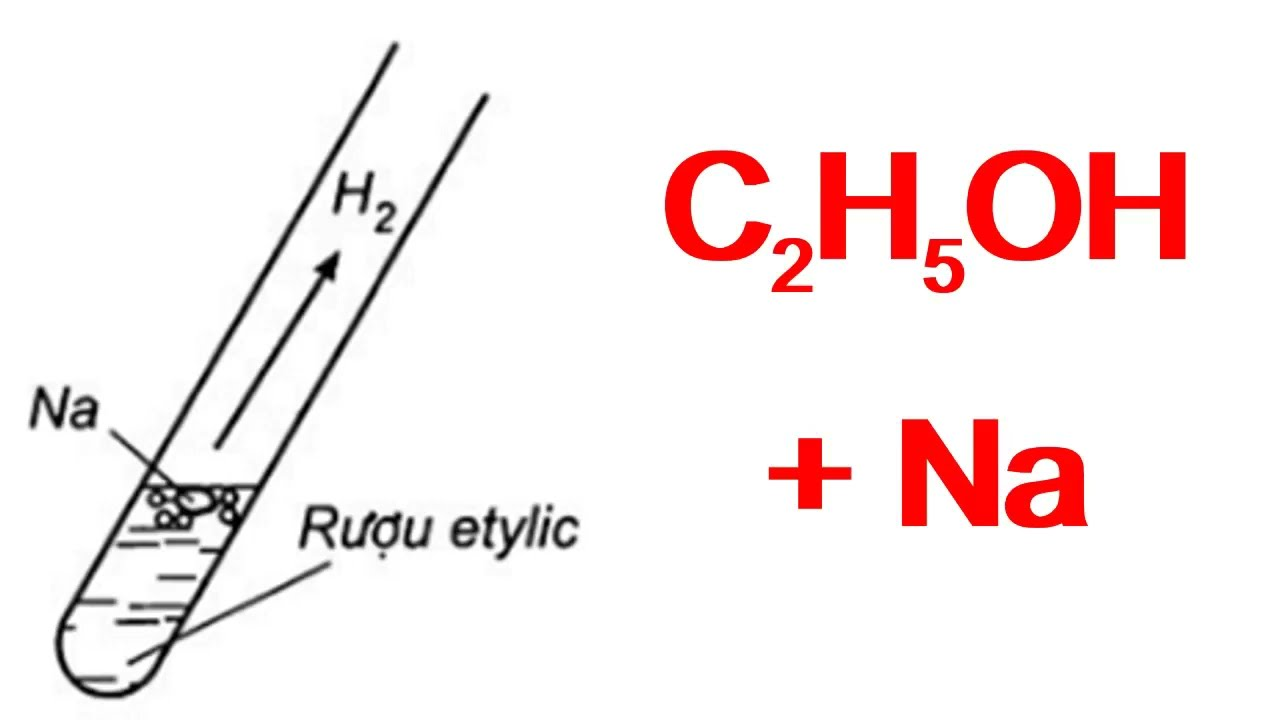
Câu 5. Cho rượu etylic nguyên chất tác dụng với kali dư. Số phản ứng hóa học xảy ra là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 6. Cho rượu etylic 80o tác dụng với natri dư. Số phản ứng hóa học xảy ra là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 7. Nhận xét nào sau đây là sai?
A. Rượu etylic là chất lỏng, không màu.
B. Rượu etylic tan vô hạn trong nước.
C. Rượu etylic có thể hòa tan được iot.
D. Rượu etylic nặng hơn nước.
Câu 8. Độ rượu là
A. số ml rượu etylic có trong 100 ml hỗn hợp rượu với nước.
B. số ml nước có trong 100 ml hỗn hợp rượu với nước.
C. số gam rượu etylic có trong 100 ml hỗn hợp rượu với nước.
D. số gam nước có trong 100 gam hỗn hợp rượu với nước.
Câu 9. Rượu etylic tác dụng được với dãy hóa chất là
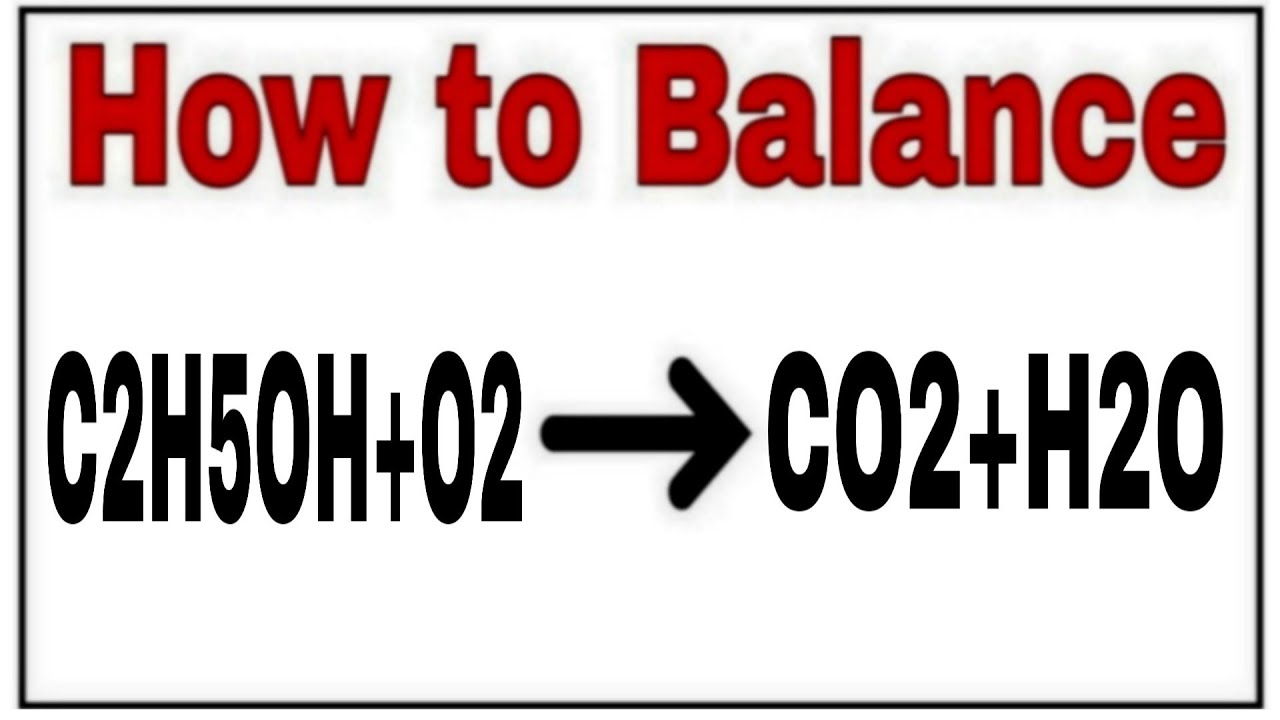
A. NaOH; Na; CH3COOH; O2.
B. Na; K; CH3COOH; O2.
C. C2H4; K; CH3COOH; Fe.
D. Ca(OH)2; K; CH3COOH; O2.
Câu 10. Trong 100 ml rượu 40° có chứa
A. 40 ml nước và 60 ml rượu nguyên chất.
B. 40 ml rượu nguyên chất và 60 ml nước.
C. 40 gam rượu nguyên chất và 60 gam nước.
D. 40 gam nước và 60 gam rượu nguyên chất.
Câu 11. Công thức cấu tạo của rượu etylic là
A. CH2 – CH3 – OH.
B. CH3 – O – CH3.
C. CH2 – CH2 – OH2.
D. CH3 – CH2 – OH.
Câu 12. Đốt cháy hoàn toàn m gam hỗn hợp 3 ancol đơn chức, thuộc cùng dãy đồng đẳng, thu được 7,612 lít khí CO2 (đktc) và 10,8 gam H2O. Giá trị của m là
A. 5,42.
B. 7,42.
C. 9,44.
D. 4,72.
Câu 13. Cho 9,2 gam C2H5OH tác dụng với lượng dư Na sau phàn ứng hoàn toàn thu được V lít khí H2(đktc). Giá trị của m là
A. 2,24.
B. 3,36.
C. 4,48.
D. 6,72.
Câu 14. Hòa tan m gam ancol etylic (D= 0,8 gam/ml) vào 216 ml nước (D= 1 gam/ml) tạo thành dung dịch A. Cho A tác dụng với Na dư thu được 170,24 lit (đktc) khí H2. Dung dịch A có độ rượu bằng bao nhiêu?
A. 40o
B. 46o
C. 36o
D. 30o
Câu 15. Nhận xét nào sau đây là sai
A. Rượu etylic là chất lỏng, không màu
B. Rượu etylic tan vô hạn trong nước
C. Rượu etylic có thể hòa tan được iot
D. Rượu etylic nặng hơn nước
Câu 16. Nhận định nào sau đây sai?
A. Có thể dùng glucoszơ để sản xuất rượu etylic.
B. Có thể dùng xenlulozơ đê sản xuất thuốc súng.
C. Phân biệt tinh bột và xenlulozơ bằng phản ứng tráng gương.
D. Phân biệt mantozơ và saccarozơ bằng phản ứng tráng gương.
Câu 17. Có 4 dung dịch: Natri clorua, rượu etylic (C2H5OH), axit axetic (CH3COOH), kali sunfat đều có nồng độ 0,1 mol/l. Khả năng dẫn điện của các dung dịch đó tăng dần theo thứ tự nào trong các thứ tự sau:
A. NaCl < C2H5OH < CH3COOH < K2SO4
B. C2H5OH < CH3COOH < NaCl < K2SO4
C. C2H5OH < CH3COOH < K2SO4 < NaCl
D. CH3COOH < NaCl < C2H5OH < K2SO4
Câu 18. Nhận xét đúng về khí etilen
A. Là chất khí không màu, có mùi hắc
B. Là chất khí không mùi, ít tan trong nước
C. Là chất khí nặng hơn không khí
D. Là chất khí không màu, ít tan trong nước
Câu 19. Hãy chọn phát biểu đúng nhất về hoá học hữu cơ trong số các phát biểu sau:
A. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon.
B. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon, trừ cacbon (II) oxit, cacbon (IV) oxit, muối cacbonat, xianua, cacbua.
C.Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon, trừ cacbon (II) oxit, cacbon (IV) oxit.
D. Hoá học hữu cơ là ngành hoá học chuyên nghiên cứu các hợp chất của cacbon trừ muối cacbonat.
Câu 20. Cho hỗn hợp các ankan sau: pentan (sôi ở 36oC), heptan (sôi ở 98oC), octan (sôi ở 126oC), nonan (sôi ở 151oC). Có thể tách riêng các chất đó bằng cách nào sau đây?
A. Kết tinh.
B. Chưng cất
C. Thăng hoa.
D. Chiết.
Đáp án B